ブリッジレポート:(4597)ソレイジア・ファーマ vol.3
| (4597:東証マザーズ) ソレイジア・ファーマ |
|
||||||||
|
||||||||
企業名 |
ソレイジア・ファーマ株式会社 |
||
社長 |
荒井 好裕 |
||
所在地 |
東京都港区海岸1-2-20 汐留ビルディング |
||
決算期 |
12月末日 |
業種 |
医薬品(製造業) |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2016年12月 | 501 | -462 | -494 | -474 |
| 2015年12月 | 229 | -702 | -710 | -643 |
| 2014年12月 | 11 | -702 | -701 | -677 |
| 株式情報(1/11現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
荒井社長率いる実務経験豊富な開発スタッフ、開発成功確率の高さ、安定した事業基盤、事業の早期実現可能性などが大きな強み・特長。 (※)スペシャリティ・ファーマ:得意分野において国際的にも一定の評価を得る研究開発力を有する新薬開発企業のこと。
 【1-2 企業理念・経営理念】
社名のソレイジア(SOLASIA)は、Sol(ラテン語で太陽)+Asia(アジア地域)からなるもので、「日本・アジアにおいて、がんと向き合うさまざまな人たちの未来を照らす希望の太陽でありたい。」という想いを表している。以下のような、『経営理念:ミッション、ビジョン、バリュー』を掲げている。   また、現在は研究開発が先行しているため財務CFに頼らざるを得ない現状であるが、早期に営業CF黒字化を実現し、持続的成長が可能な基盤を構築する。 【1-3 同社を取り巻く環境】
厚生労働省「平成27年(2015)人口動態統計」によれば、2015年の死因別順位は悪性新生物(がん)が、死亡数370,346人で全死亡者数1,290,444人の28.7%を占め第1位であった。総人口の変化を加味した「死亡率(人口10万人に対し何人が死亡したか)」の推移を見ても、1981年に死亡率142.0人で、同134.3人の脳血管疾患に代わり第1位となって以来30年以上にわたり連続して第1位であり、その数値も年を追って上昇、2015年は295.5人となっている。 高齢化、また食生活を含めたライフスタイルの変化等によりがん発症率は上昇していると言われているが、中国においてもがんの発症者数及び死亡者数は増加傾向にある。 現在の国別医薬品市場規模は1位が米国で、中国が第2位だが、2020年には中国市場は米国市場と1位を分け合う規模まで拡大するとも言われている。 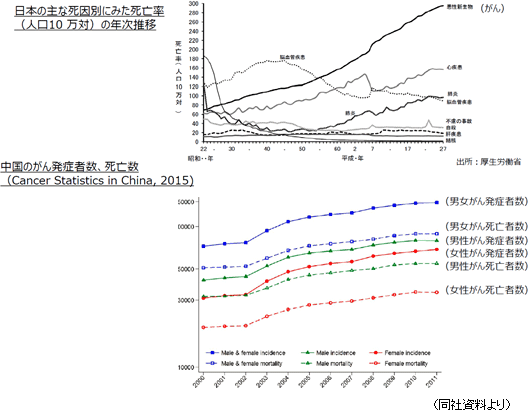 (新規抗がん剤) 抗がん剤を用いたがん治療においては、一つの抗がん剤のみを用いる単剤治療よりも、複数の抗がん剤を用いる併用療法のほうがより高い効果を期待できるといわれている。 加えて、がんは種類によって異なるが、再発の可能性が高く、加えて難治の場合は、一種類の治療での治癒は困難であるため、一つの治療薬が絶対的な存在とはならず、他の治療薬が直接的な「競合」とはなり難いという特性がある。 また、近年では、分子標的薬や免疫療法が注目されてはいるが有効性や普及という意味では、まだ緒に就いたばかりであり、伝統的な殺細胞性抗がん剤が標準治療として位置づけられている。 (がんサポーティブケア) 抗がん剤はがん細胞を攻撃する強力な医薬品であり副作用が避けられない。 患者に負担がかかる副作用をコントロールできなければ、抗がん剤投与によるがん治療そのものを中止せざるを得ず、結果的にはがんが進行してしまう。 こうした事態を避け、がん治療を完遂するためには、副作用のコントロールを行うための医薬品や医療機器への期待が高まっている。 また、がんの治療薬は、がんの種類ごとに承認を得なければならないが、サポーティブケアはがんの種類を問わず、幅広いがん患者への処方が可能であり、大きなニーズ、市場が見込まれる。 以上のように、日本・中国におけるがん治療ニーズの増大とそれに対応した新規抗がん剤およびがんサポーティブケアへの期待は大きく、同社はこうしたニーズを取り込み、収益を拡大させるためのビジネスモデル、事業戦略を構築している。 【1-4 事業内容】
(1)ビジネスモデル
新しい医薬品が上市されるまでには、「基礎研究」から始まり、「製剤研究」、「非臨床開発(動物を用いて薬効薬理作用、生体内での動態、有害な作用などを調べる試験)」、「臨床開発(医薬品や治療技術などの人間への影響を調べる科学的試験)」を経て、当局の承認を得たのち、「製造」、「販売・マーケティング・製造販売後調査」といったプロセスを経るのが一般的である。大手製薬会社は、巨額な研究開発費を変動費化することなどを目的にCROを利用した臨床開発段階のアウトソーシングを進めてはいるが、基本的には上記の工程全てを自社内に保有している。 これまではこうした体制が製薬会社の高収益体制を支えてきたが、近年の生命科学分野の急速な進歩や複雑化、多様化により、自社固有の創薬技術が陳腐化してしまう可能性が高まっている。 また、多額の費用と時間をかけて基礎研究から進めても臨床開発に入るまでに実用化を断念し、創薬技術を確立できないケースも多く、医薬品開発には常に高いリスクがついてまわる。 そこで同社では、失敗の確率の高い基礎研究から非臨床開発の工程を自社では行わず、まだ開発段階にある将来有望な医薬品を外部から導入して臨床開発から開発に着手。それ以降の事業活動に経営資源を集約することで自社の強みを発揮するとともにリスクの低減を図っている。 現時点ではコスト負担の大きい製造工程も保有しない計画である。  一般的に製薬企業の売上高総利益率は高水準であるが、これは、製造および販売活動を内製化することによって実現できると考えられる。  そこで同社では、臨床開発を終えた医薬品について、「自販モデル」と、販売権を他社に導出する「導出モデル」を併用している。 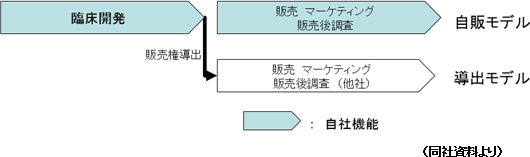 中国の3大都市「北京・上海・広州」においては自社販売体制を構築し自販モデルを展開する。 この3都市の人口合計は中国全人口の約5%に過ぎないが、抗がん剤を取り扱うのは最先端かつ大病院であるため、大病院が集中するこの3都市は中国の抗がん剤市場の3割を占める巨大マーケットである。 また、新しい医薬品の使用・普及にあたっては影響力のある医師の判断や決定がその結果を大きく左右する。こうした影響力のある医師の在籍する大病院への営業活動は極めて重要なポイントとなる。 加えて、中国全土ではなくあくまでもそれぞれの都市における営業であり、少人数の販売組織でも十分に活動は可能である。現在約50-60の大病院を対象とした営業スタッフ増強に動いている。 (導出モデル) 現在の主な導出先パートナーは以下の2社である。  (2)開発パイプライン
現在、前述の経営方針に沿って以下4つの開発パイプラインを有している。
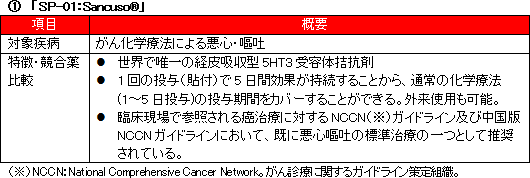 (対象疾病の概要)
抗がん剤の代表的な副作用として悪心や嘔吐はよく知られている。抗がん剤を投与すると、小腸にあるクロム親和性細胞と呼ばれる細胞がダメージを受ける。 ダメージを受けたクロム親和性細胞はセロトニンという神経伝達物質を放出。これが末梢の迷走神経上にある5-HT3受容体に取りこまれ、その刺激が末梢の迷走神経に沿って、脳の第4脳室最後野にある化学受容器引金帯(CTZ)を介して延髄に入り、悪心・嘔吐の命令を生体に出す嘔吐中枢を刺激し、悪心や嘔吐が発現する。 悪心・嘔吐を抑制するためにはセロトニンによる5-HT3受容体への刺激を遮断することが必要であり、そのために用いられる薬剤「5-HT3受容体拮抗薬」としては様々なものがあるが、代表的な薬剤がグラニセトロンである。 (「SP-01」概要)
「SP-01」は、このグラニセトロンを含んだ5-HT3受容体拮抗薬の経皮吸収型製剤(貼付剤)で、貼り薬としては世界唯一。
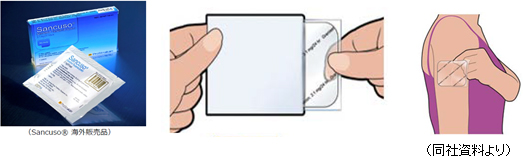 これに対し「SP-01」は5日間にわたって安定的に血中のグラニセトロン濃度を維持することができるため、1回貼り付ければ制吐剤を追加する必要がなく、入院ではなく外来によるがん治療を可能とするため、患者のQOL向上にも大きく貢献する。 悪心・嘔吐、口内炎などが原因で、薬剤の服用が困難な状態にある場合でも、経皮吸収型製剤は使用可能である点も大きなメリットであり、以上のような点を評価され、米国NCCN診療ガイドライン、中国治療ガイドラインで処方推奨を得ている。 現在上市または承認済の地域は、米国、英国、ドイツ、オランダ、デンマーク、スペインフィンランド、ノルウェー、スウェーデン、クウェート、レバノン、カタール、バーレーン、アラブ首長国連邦リビア、サウジアラビア、韓国、フィリピン、オーストラリア(以上、導入元が販売)、台湾、香港、シンガポール(以上、サブライセンス先の協和発酵キリンが販売)など多数にわたっている。 今後は、抗がん剤だけでなく放射線療法による悪心・嘔吐抑制への適応拡大を見込んでいる。  (対象疾病の概要)
悪性リンパ腫は、血液がんの1つで、白血球の中のリンパ球ががん化したもの。リンパ球には、B細胞、T細胞、NK細胞等の種類があり、これらががん化して無制限に増殖することで発症する。 末梢性T細胞リンパ腫(PTCL:Peripheral T-cell lymphoma)とは、悪性リンパ腫の種類の1つ。リンパ球の中のT細胞から発生するもので、月単位で病気が進行する「中悪性度」に分類され、中悪性度リンパ腫の10~15%を占めるといわれている。 B細胞リンパ腫などに比べ、5年生存率は低く、25%前後である。 (「SP-02」概要)
「SP-02」は、この末梢性T細胞リンパ腫(PTCL)への適応で開発をスタートさせた。2015年10月までに米国や日本、韓国等にて187名の被験者に投与される実績を有する。 米国における前期第II相臨床試験は2012年4月に完了し、白人種における一定の有効性を確認した。 2015年4月に完了した日本および韓国における第Ⅰ相臨床試験では、競合品と比較して高い安全性が確認され、アジア人種における一定の有効性が示唆された。 悪性リンパ腫はしばしば再発することが知られており、作用機序の異なる複数の治療薬が必要でマーケットは大きいと同社は考えている。 末梢性T細胞リンパ腫のみでなく、その他血液がん(リンパ腫、白血病)や固形がんへの適応拡大を目指しており、2019年以降の開発開始を予定している。 日本での開発販売権はMeiji Seika ファルマ株式会社に導出済で、欧米及び中国では導出先を選定中である。  (対象疾病の概要)
抗がん剤による悪心・嘔吐と並んで、癌化学療法又は放射線療法による口腔粘膜傷害の副作用も患者にとっては大きな困難である。口内炎は、「化学療法が口腔粘膜へ直接作用して障害が生じるもの」や「放射線照射により唾液腺組織に障害が生じ、唾液の分泌低下により口腔内の自浄作用が低下し局所感染が起こることで発生するもの」である一次口内炎と、「白血球減少などに伴う骨髄抑制により起こる口腔内感染が原因となるもの」である二次口内炎がある。 抗がん剤治療に伴う口内炎の発生頻度は30~40%、抗がん剤と頭頸部への放射線治療併用時の口内炎発生頻度は約100%となっている。 癌化学療法又は放射線療法による口内炎は、300~500もの多数の炎症が発生する。その疼痛により患者は食事や水分の経口摂取が困難になり体力低下を招き、重症化すると本来のがん治療の継続にも悪影響を及ぼしてしまう。 ただ、現在のところ標準的な対処法はなく、各病院ごとでの対症療法に頼っているのが現状である。 (「SP-03」概要)
「SP-03」は、脂質ベースの液体を口腔粘膜に吹きかけるものであり、同社ではカテゴリーとしては医療機器として開発を進めてきた。
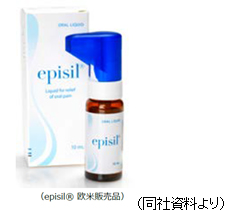 2016年に日本における承認申請を完了していたが、2017年7月6日付けで、厚生労働省より、日本国内における医療機器製造販売承認を取得した。今後、保険収載を経て、日本における独占販売権の導出先であるMeiji Seika ファルマ株式会社より販売が開始される予定だ。 なお、中国においても2016年5月に医療機器製造販売承認申請を当局に行っており現在承認審査中だ。 日本以外では、米国、英国、ドイツ、デンマーク、ノルウェー、スウェーデンなどで他社及び導入元により販売されている。  早期の承認取得を実現するため、まず大腸がん治療における代表的な抗がん剤「オキサリプラチン」投与による末梢神経障害に適応を絞り、日本や中国など東アジア地域での臨床開発を進めていく。 (対象疾病の概要)
がん化学療法は、悪心・嘔吐や口内炎発症等の副作用が生じるが、末梢神経障害も重篤な副作用の一つ。末梢神経障害は、プラチナ製剤やタキサン製剤等のがん化学療法の主要薬剤において、顕著に発現することが知られている。 大腸がんのうち手術による治癒が難しい進行・再発がん(ステージIII、Ⅳ)に対する化学療法及び術後補助化学療法における代表的な治療法であるFOLFOX療法は、フルオロウラシル・フォリン酸・オキサリプラチンの 3 剤を併用するものだが、このうちオキサリプラチンの処方は、患者の約9割で「手、足や口唇周囲部等の異常感覚」、「呼吸困難や嚥下障害を伴う咽頭喉頭の絞扼感(しめつけ)」、「手足先のしびれ」、「感覚低下」、「感覚性運動失調」などの症状を伴う末梢神経障害を生じさせる。 このような副作用が発現した場合には、薬剤中止により、80%の症例では一部症状の改善がみられ、40%の症例では 6~8 ヶ月後には完全に回復するが、薬剤中止はがん化学療法の中止や方針変更となる可能性があり、末梢神経障害の治療は医療上の重要な課題である。 ただ、がん化学療法の副作用としての末梢神経障害を適応として当局に承認された医薬品は現時点では存在していない。 (「SP-04」概要)
「SP-04:PledOx®」の導入元Pled 社はストックホルム証券取引所に上場しており、酸化ストレス関連の疾患に対する医薬品開発に強みを持つ。「PledOx®」(一般名:Calmangafodipir)は欧米で販売実績を有するMRI造影剤「Mangafodipir」を基に創生された新有効成分である。 後述のように「SP-04:PledOx®」は後期第II相臨床試験を終了し、今後、第III相国際共同臨床試験が開始される予定で、末梢神経障害薬のトップランナー。開発成功は大きな先行者利益獲得につながるだけでなく、がん患者のQOL向上など社会的貢献度も高い。 *市場性 ソレイジア・ファーマによれば、FOLFOX療法の対象となる大腸がん患者数は年間で日本6~10万人、中国20万人程度と推定している。 FOLFOX療法は、「3日間の治療、11日間の休薬期間」の計14日間が1サイクルであり、それを12サイクル行う治療法である。 対象疾患はオキサリプラチン投与を含むがん化学療法の対象となる大腸がんであるが、オキサリプラチン以外のプラチナ製剤やタキサン製剤等のがん化学療法の主要薬剤においても末梢神経障害が顕著に発現することがしられており、乳がん、肺がん、卵巣がん、膵臓がんなど大腸がん以外の固形がんも追加対象疾患となれば、市場性は更に広がると同社は想定している。 *開発状況 Pled 社は、これまで末梢神経障害を適応として PledOx®の研究開発を欧米で行ってきており、後期第II相臨床試験までの結果、FOLFOX療法を受けている進行性大腸がん患者において、有効性と安全性、つまり末梢神経障害を改善する効果およびFOLFOX 療法によるがん治療そのものへの影響を生じさせないこと等についての効果が示唆されている。 現在、Pled 社は、米国で日本人を被験者とするPledOx®の第Ⅰ相臨床試験を実施しており、ソレイジア・ファーマはそれ以降の臨床開発をPled 社の行ってきた他の研究開発結果とともに引き継ぐ。 (Pled社が日本への導出を検討した際、日本人を対象とした臨床試験が必要と判断したため。) Pled 社は、FDA(米国食品医薬品局)及び EMA(欧州医薬品庁)との協議を経た第III相国際共同臨床試験への被験者登録を今後開始する予定である。 現在Pled社が米国で実施中の日本人を被験者とする第Ⅰ相臨床試験は2018年初頭には終了する予定であり、ソレイジア・ファーマはその後日本当局と協議の上、この第III相国際共同臨床試験に参画したいと考えている。 以上4つのパイプラインの開発・事業化の経緯、現状、今後の計画は以下のとおりである。  【1-5 バイオベンチャーとしての6つの特徴】
バイオベンチャーとしての同社を特徴づけるのは主に以下の6点である。
① 創業の経緯
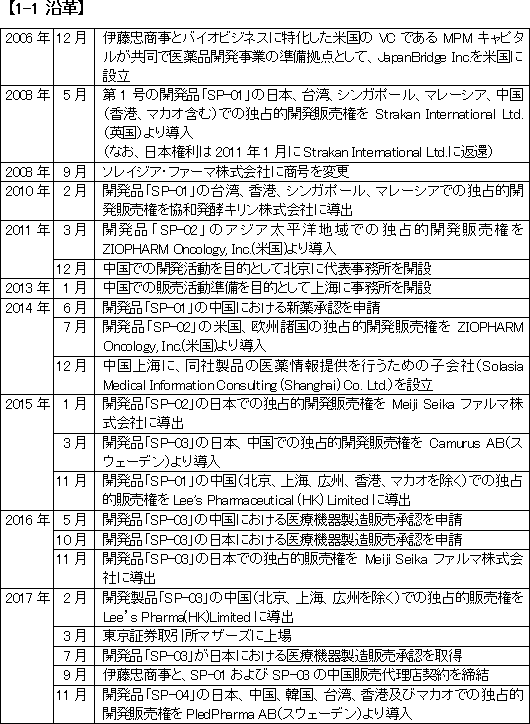
同社のスタートは、伊藤忠商事と米国のバイオに特化したVCであるMPMキャピタルによって設立された「JapanBridge (Ireland) Limited」。数社のバイオベンチャーから新薬の権利を導入し、開発を進めた。当初はExitとして製薬会社への売却を中心に考えていたが、4-5年ほど前からは事業の将来性、有望性から企業として永続的に事業を展開する方向にシフトし、研究開発に向けた資金調達も必要なため株式公開の道を選択した。 もともと他社への売却を念頭に置いていたことから、保有する開発品は開発段階ではあっても他社に売却して現金化可能な優良な資産で構成されており、創業時より既に強固な事業基盤を構築している。 ② 実務経験豊富な臨床開発陣 研究部門や前臨床部門を持たず、新薬開発の権利導入を活用し、臨床開発以降の医薬品創造プロセスに特化している。医薬品事業化への研究開発過程において最も大切なのは最終的に当局の承認を取得することであるが、そのためには臨床開発、特に第II相以降の後期臨床段階におけるスキルやノウハウが最も重要である。 数多い日本のバイオベンチャーの中でも、社長が臨床開発をコアスキルとして身に付け、強力な武器としているのは同社荒井社長以外には見当たらない。 荒井社長率いる実務経験豊富な臨床開発スタッフは同社の強力な差別化要因、競争優位性である。 ③ 開発成功確率の高さ 直近導入した「SP-04」に先立ち、「SP-01」、「SP-02」、「SP-03」という3つの開発品を導入しているが、開発中止や失敗実績はなく、3つの開発品全てが事業化に至る最終段階(1つは日本で承認取得、1つは承認申請済、1つは最終臨床試験実施中)にある。 この高い開発成功確率を可能にしているのは2つの要因である。 1つ目は、失敗のリスクの低いもののみを導入するビジネスモデル。 2つ目は、臨床開発のすべてを担うことのできるチームが社内にあること。前述のように、承認を取るためには何が必要かを熟知した開発陣は、導入品が承認をとれるか否かについてのスクリーニングをかけることができる。 1つ目、2つ目を合わせた、いわば「目利き力」が、開発断念に至るリスクを引き下げ、3打数3安打という高打率の源泉となっている。 新薬のキャッシュインフローをDCF(ディスカウント・キャッシュフロー)モデルから分析してみると、将来にわたるトータルのキャッシュインフローの大部分を構成するのは契約金やマイルストンではなくロイヤルティであるが、言うまでもなくロイヤリティは最終的に開発が成功し、販売が拡大しないと獲得することはできない Pled社への提案に際し、多くの競合に比べ、契約金を始めとした金額面では決して有利ではなかったにもかかわらず今回「SP-04」を導入できたのも、明確な臨床開発設計を構築できるチーム力、先行3製品の開発実績、日本・中国を含めたアジアでの実績などをPled社が評価し、ソレイジア・ファーマがアジアにおける「PledOx®」成功のためのベストパートナーと判断したものであろう。 ④ 安定した事業基盤 前述のように開発品3つ全てにおいて、製薬企業への販売権導出を達成しており、自社販売と組み合わせたリスクヘッジのためのポートフォリオを構築済である。 ⑤ 高利益確保のための自販体制 製薬会社が高い収益性を実現できているのは、自社で製造・販売双方を手掛けているためだ。 同社は現在のところ製造設備は保有していないが、収益性を高めるためにマーケットが大きくかつ効率的に営業活動が展開できる中国の三大都市(北京、上海、広州)に自社販売体制を構築中である。 ⑥ 事業の早期実現 バイオベンチャーの場合、新薬開発段階では損失を計上しているのが一般的であるため、株価や事業価値の算定において損益計算書を使用することは合理的ではなく、DCFモデルを使用することとなるが、バイオベンチャーを対象とする場合、通常のDCFで使用される「時間」を基にした割引率以外に、新薬の臨床段階ごとの成功確率が割引率として考慮される。この場合、承認をいつ得ることができるかが最大のポイントとなるが、3つの開発品のうち、「SP-03」は既に承認を獲得し、「SP-01」は2018年12月期上半期での承認を予定している同社の新薬開発に関する割引率は、他のバイオベンチャーよりも低く想定されてしかるべきであろう。 以上6点以外に中国市場での成長ポテンシャルの高さを挙げることができる。 世界のメガファーマも当然中国をはじめとしたアジア各国に拠点を設けているが、同社が開発の対象とするのは経営方針にあるように、大手製薬企業が業績重視の観点から着手しないがん領域や希少疾病領域での新規製品である。近年医薬品市場で注目を浴びるこうした製品はバイオベンチャー発のものであるが、大手は取り扱わないため、同社は、北京・上海・広州の自社販売網を含め、世界中のバイオベンチャーにとって急成長するアジア市場へのアクセスを提供できる貴重な存在となろう。加えて、中国ビジネスに強みを持ち筆頭株主である伊藤忠商事と香港、マカオを除く中国全土における販売代理店契約を締結し、そのネットワークを活用できる点も同社の大きなアドバンテージである。 |
| 2017年12月期第3四半期決算概要 |
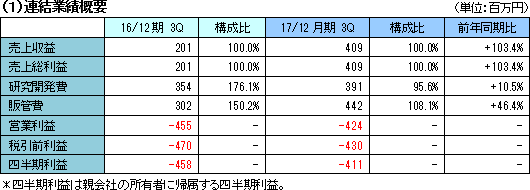 「SP-03」のマイルストン収入があるも事業化のための先行投資で営業損失
売上収益は4億9百万円。「SP-03」の日本国内における医療機器製造販売承認取得に基づくマイルストン収入4億円をMeiji Seika ファルマより受領したほか、「SP-01」の製品販売純収入が9百万円。前年同期の主な売上収益は「SP-02」のマイルストン収入2億円。営業損失は4億24百万円。臨床試験の推進を中心とする医薬品開発パイプラインの強化と事業化に注力し、研究開発を進めたほか、開発及び株式公開のための体制整備のコストにより営業損失が生じている。 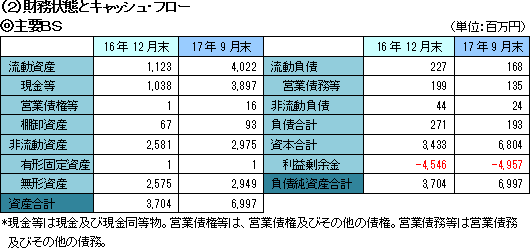 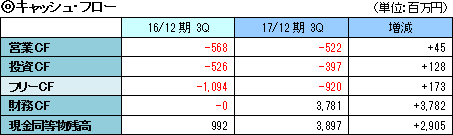 (3)トピックス
◎当座貸越契約を締結
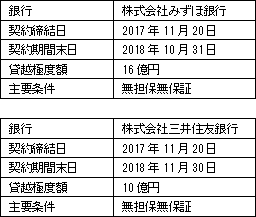
同社は新規開発品「SP-04」導入投資としてPled社への契約に基づく支払いのほか、「SP-04」臨床開発等への投資を行っていく必要がある。上場時公募増資等により調達した資金は、主として既存開発品の 「SP-01」、「SP-02」、「SP-03」の開発費用及び事業化準備費用に充当し、その一部を新規開発品に充当する。この上場時公募増資等により調達した資金に加え、「SP-04」への当面の投資資金を確保するために、メガバンク2行と当座貸越契約を締結した。
 |
| 2017年12月期業績予想 |
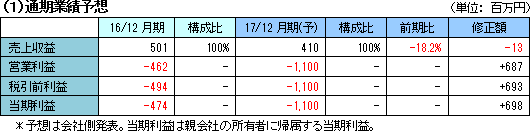 中国における「SP-01」承認時期のずれにより業績予想を変更。
17年12月22日、業績予想を修正した。「SP-01」の中国当局の承認予定時期を従来は今期中と見込んでいたが、審査手続きが遅延しており来期上半期での取得見込みとしたため。売上収益は前期比18.2%減少の4億10百万円の予想で13百万円の下方修正。中国当局承認を契機として受領を予定していたマイルストン収入を除外する。 営業利益は11億円の損失の予想で6億87百万円の上方修正。「SP-01」承認時期のずれにより投資活動が限定され費用発生が抑制される。 |
|
| <参考:コーポレートガバナンスについて> |
 ◎コーポレートガバナンス報告書
最終更新日:2017年10月20日<実施しない主な原則とその理由> 「当社は、コーポレートガバナンス・コードの基本原則をすべて実施しています。」と記載している。 |
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2025 Investment Bridge Co.,Ltd. All Rights Reserved. |





