ブリッジレポート:(4549)栄研化学 vol.7
| (4549:東証1部) 栄研化学 |
|
||||||||
|
||||||||
企業名 |
栄研化学株式会社 |
||
代表執行役社長 |
和田 守史 |
||
所在地 |
東京都台東区台東4-19-9 山口ビル7 〒110-8408 |
||
決算期 |
3月末日 |
業種 |
医薬品(製造業) |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2016年3月 | 32,163 | 3,536 | 3,570 | 2,429 |
| 2015年3月 | 31,014 | 2,826 | 3,013 | 2,100 |
| 2014年3月 | 30,027 | 3,008 | 3,095 | 1,984 |
| 2013年3月 | 28,645 | 2,548 | 2,812 | 2,453 |
| 2012年3月 | 27,702 | 2,363 | 2,543 | 1,460 |
| 2011年3月 | 27,562 | 2,709 | 2,775 | 1,672 |
| 株式情報(5/27現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
国内シェア約57%の便潜血検査用試薬を始め、尿検査用試薬や微生物検査用試薬など他社にはない独自技術・ノウハウを利用した高シェア製品多数。また独自開発の遺伝子増幅技術「LAMP法」は世界的に高い評価を得ている。便潜血検査、尿検査とLAMP法などの独自技術を武器にグローバル企業への成長を目指している。 【沿革】
【経営理念】
*経営理念: 「ヘルスケアを通じて人々の健康を守ります。」
*経営ビジョン:「EIKENグループは、人々の健康を守るために、検査のパイオニアとしてお客様に信頼される製品・サービスを提供し、企業価値の向上を図ります。」
*モットー: 「品質で信頼され、技術で発展する“EIKEN”」これらを中心に各ステークホルダーへの考え方として、EIKEN WAYを策定している。  【市場環境】
臨床検査薬市場は、2014年度で約3,370億円、研究用試薬と検査用機器を含めると約5,573億円(一般社団法人日本臨床検査薬協会調査)となっている。<国内市場> 行政は増大している医療費を抑制するために特定健診(メタボ健診)やがん検診の受診率向上やOTC検査薬(薬局で購入できる検査薬)の規制緩和といった予防医療に力を入れており、今後、高齢化の進展と共に臨床検査数(検体数)の増加が見込まれる。 一方でマイナス面としては、価格競争による単価の低下、診療報酬改定(引き下げ)及び長期的には少子化による人口減少がある。ただ、診療報酬改定の対象である保険(検体検査実施料)の推移を見ると、1997年から2006年までの期間に約4割引き下げられたものの、その後はほぼ横ばいないし微減となっている(平成28年度検体検査実施料 -0.4%)。これは同社の含めた業界全体として予防、検査の重要性を働きかけた結果という事で、中期的には国内市場は年率3%程度の微増傾向が続くと思われる。 矢野経済研究所による「臨床検査市場の展望2009年版」によると、同社は、シスメックス(6869、東証1部)、ロシュ・ダイアグノスティックス(独ロシュグループの日本法人)、富士レビオ(現 みらかホールディングス。4544、東証1部)、アボットジャパン(米アボットグループの日本法人)につぐ第5位、シェア5.8%となっている。 前述の協会会員126社(2016年4月時点)の内メーカーは約80社で、売上100億円以上の企業は15社程度となっており、大多数は中堅・中小企業という構造。臨床検査は検査項目が多岐にわたっているため企業ごとに得意とする分野が異なり、企業間での棲み分けが出来ている。そのため、他社から原料・製品を仕入れて製造・販売するといった業務提携が多く見られる。また、そうした棲み分けが出来ている中、市場は小幅ながらも拡大しているため、明確な淘汰は現在のところ起きていないということだ。 <海外市場>
2014年の世界の検体検査薬・機器市場は約560億USDといわれており、地域別構成比は米国42%、欧州32.7%、アジア・パシフィック22%などとなっている。市場規模自体が国内市場の10倍超と巨大であると同時に、先進国では高齢化の進展に伴う検査数の増加、また新興国においては経済成長、所得増加に伴う医療ニーズの拡大などにより、年率7~8%と国内市場を大きく上回る成長が見込まれるため、国内の各関連企業は積極的にグローバル化を進めている。 ただ、グローバル市場においては、ロシュ、アボット、シーメンス、ベックマンなど売上高が2,000~9,000億円にも上る世界的大企業がメインプレーヤーとなっており、日本企業が競争に勝ち抜くためには独自性のある製品・システムの開発など競争力強化が不可欠である。 【事業内容】
1.臨床検査とは
臨床検査には、レントゲン、CT、MRI、心電図、超音波など、医療機器を使用して体を直接調べる「生体検査」と、患者から採取した血液、尿・便、細胞などの生体試料(検体)を調べる「生理機能検査(検体検査)」がある。同社が取り扱う臨床検査薬とは、検体検査に使用する試薬の事で、例えば感染症の検査や便に含まれる微量の血液の測定など、病気の診断をサポートするもの。これら試薬の大部分は体外診断用医薬品と呼ばれ、医薬品医療機器等法の規制を受け、試薬メーカーなどがPMDA(医薬品医療機器総合機構)に対し申請し、認可を受けたものである。ユーザーは、病院、医院、診療所、受託を受けて検査を行う検査センター、健診センター、保健所、衛生検査所など。 2.主力製品
主として以下の各検査用試薬や測定装置を製造・販売している。同社は幅広い検査薬を取り扱うために、自社製品に加え他社製品の仕入販売も行っている。 主要な自社製品は、便潜血検査用試薬、微生物検査用試薬、免疫血清検査用試薬、尿検査用試薬、遺伝子検査用試薬など。自社製品と他社製品の売上比率は約60:40。粗利率は自社製品が約55%、他社製品が約35%。  便潜血検査用試薬
大腸がんのスクリーニング検査として糞便中ヒトヘモグロビンを特異的に検出・測定する便潜血検査用試薬・採便容器を主力製品とし、グローバルに販売している。
免疫血清検査用試薬(便潜血検査を除く)
リウマチや炎症性疾患の診断及び胃の健康度評価(ABC分類)に使用する汎用自動分析装置用試薬「LZテスト‘栄研’」を始め、各種検査用試薬の開発、製造、販売を行っている。また東ソー(株)から、全自動エンザイムイムノアッセイ装置用試薬及び自動グリコヘモグロビン分析装置用試薬を導入・販売している。 尿検査用試薬
尿中の潜血、たんぱく質、ブドウ糖など多項目の検査が行える尿検査用試験紙「ウロペーパーIII‘栄研’」、全自動尿分析装置用には専用試験紙の「ウロペーパーαIII‘栄研’」などを開発・製造・販売している。
微生物検査用試薬
同社は創立以来、感染症及び食中毒の予防を目的とし、生体試料や食品・環境の微生物検査用試薬を開発してきた。現在では、各種細菌検査用培地(増菌用培地、分離用培地、生物学的性状検査用培地、同定検査用培地)、薬剤感受性検査用試薬、迅速検査キットなど、微生物感染症の診断・治療に有用な各種検査用試薬を開発・製造・販売している。
生化学検査用試薬
生活習慣病との関連性が注目されている検査項目を中心に、血清や尿を検体とし生体成分を測定・分析する「エクディアXL ‘栄研’」シリーズなど、生化学検査用自動分析装置に対応する各種検査用試薬を開発・製造・販売している。
器具・食品環境関連培地
食中毒原因微生物の検査などの食品微生物検査用試薬や作業環境の汚染実態などを把握できる環境微生物検査用試薬及び検査用器具・器材の販売を行っている。
医療機器
各種自動分析装置を販売している。自社試薬を使用する専用装置は製造委託を行っている。便潜血測定装置「OCセンサー」は1989年の発売以来、技術革新と品質向上を重ねている。また、独自技術である画像処理システムを使用した尿自動分析装置「US」、臨床検査分野で世界初となる全自動生物化学発光免疫測定装置「BLEIA-1200」、LAMP法リアルタイム濁度測定装置「LoopampEXIA」など取り揃えている。
遺伝子(LAMP法)関連
同社は1998年、新規遺伝子増幅技術LAMP法を独自開発し特許を取得し、LAMP法を利用した遺伝子検査用試薬を開発・製造・販売している。また、ライセンスも積極的に実施している。このLAMP法は、「簡易、迅速、精確」という特徴を有しており、今後のグローバル展開のための大きな武器となっている。(詳細は後述)
3.販売体制
国内の販売体制は11営業所、2営業部。学術部門が販売促進の支援を行っている。2016年3月期の全従業員686名(連結)中、約300名が営業部門。 ユーザーである病院など医療機関向けチャネルに関する直接の販売先は医療系卸会社で、殆ど全ての卸会社と取引を行っている。 海外販売においては、基本的に1か国・1代理店体制をとっており、販売とメンテナンスを委託しており、本社の海外事業室が管理している。 輸出先は43ヵ国(2016年3月期)。米国、イタリア、フランス、スペイン、韓国、台湾が海外売上の大半を占めている。 アムステルダム(オランダ)に欧州支店があるほか、中国に関しては連結子会社「栄研生物科技(中国)有限公司」での生産・販売体制の強化を行う他、中国事業室を設置しビジネス拡大を図っている。今後は規模拡大に伴い現地法人化も検討していく。 2016年3月期の海外売上高は3,498百万円。うち便潜血検査用試薬・装置は2,471百万円で構成比は70.6%。 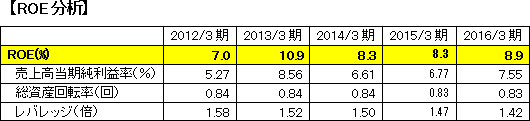 重点施策に挙げている高付加価値製品の開発、新規事業・新規市場の創出及び原価率及び販管費率の低減による利益率及び生産性向上を一段と強化する。 現在約6割の自社製品比率を7割から8割程度に引き上げることが必要なため、特に海外においてはスタッフ増強も含めた営業力の強化が必要と考えている。 (2013年3月のROEが高いのは、土地売却による特別利益を計上し売上高当期純利益率が上昇したため。) 【特徴と強み】
①高シェアの製品群
便潜血検査用試薬の国内シェアは約57%でトップであるほか、尿検査用試薬で約23%(2位)、微生物検査用試薬で約18%(2位)等と他社にはない独自技術・ノウハウを利用した多くの自社製品において高いシェアを有している。同社が便潜血検査用試薬で高いシェアを獲得することができた背景としては、1987年に発売した目視判定法用の便潜血検査用試薬「OC-ヘモディア」が、競合品に比べユーザーニーズに合致した製品であったこと、1989年には測定原理に免疫法(ラテックス凝集法)を採用し世界初の全自動分析装置「OC-センサー」を発売したことである。 また、便潜血検査は1992年に老人保健法の改正が行われ、大腸がん検診のスクリーニング検査法として公費で受診が可能(受診者負担が無料)になったのをきっかけに、普及が加速し競争が激しくなったが、同社は、機能を一新した「OC-センサーneo」を2001年に発売し、シェアを拡大してきた。 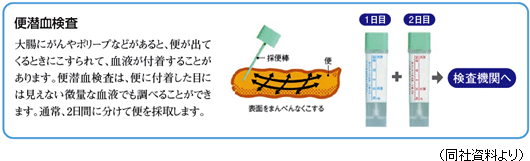 日本で実施されている免疫法は、ヒトの血液のみ反応する試薬となっており、また、自動化装置による大量処理が可能である。 一方海外では化学法による古いタイプの試薬が使用されており、精度面に課題がある。2011年になりようやく欧州の検診ガイドラインで免疫法による自動装置測定が推奨され、大きな市場の変化が表れ始めた。 また、市場が最も大きいアメリカでも化学法が主流であるが、徐々に免疫法へのシフトが始まっており、欧州、北米、アジア・オセアニアの先進国・新興国には未開拓な大きな市場が控えている。 便潜血検査市場は、ニッチな市場であるため、いち早く免疫法を開始した日本企業の技術が最も進んでおり、同社の試薬・装置がグローバルスタンダードとなっている。 ②研究開発に注力
研究開発型企業として独自性のある技術の研究開発と、それをベースとした顧客ニーズに対応したオリジナル製品の開発に注力している。研究開発要員は約100名。顧客の要望は医療のクオリティ向上。具体的には、高感度・高品質による疾患の鑑別精度の向上、検出率の改善といった点が挙げられる。加えて、使用法が簡便であれば医療従事者の負荷軽減につながるため、そうしたニーズへの対応も重要なポイントとなっている。 同社は、1939年の創業以来培ってきた試薬製造の独自技術が蓄積されており、またその試薬の性能を有効に活用するための装置に関しても、便潜血検査用装置や尿自動分析装置、生物化学発光免疫測定装置(BLEIA法)、遺伝子検査などで他社にはない独自技術が用いられている。 ③アライアンス戦略による多品種・多分野展開
臨床検査薬はその対象、項目は多岐にわたり、すべてを自社で開発・製造・販売を手掛けることは困難である。同業他社の多くは自社の得意な技術・製品に絞っているが、同社は臨床検査薬の総合メーカーとして、収益構造の安定化をめざし、アライアンス戦略を通じて自社の有する強みの拡大、機能の補完、新技術の取得といったシナジー効果を追求しつつ、広範に取扱製品を揃え、医療機関を始めとした顧客、ユーザーのニーズに対応している。多品種・多分野に展開しているもう一つの理由としては、経営理念「ヘルスケアを通じて人々の健康を守ります。」にあるように国民の健康を守るという責務を達成するためには、幅広い臨床検査に対応することが企業としての社会的責任であるとの想いも根底にある。 ④「LAMP法」の優位性
遺伝子検査の中の過程の一つである遺伝子増幅プロセスにおける現在の主流技術は「PCR法」と呼ばれるもの。これに対し同社は1998年「LAMP法」という独自技術を開発した。「LAMP法」はPCR法と比較して、以下の様な優れた特徴を持ち、簡易で迅速に特異性の極めて高い遺伝子検査を行うことが出来るものである。  同社はLAMP法の地位確立のため感染症検査に注力すると同時に、LAMP法の普及・認知度向上のために、畜産・水産、食品・環境など医療以外の分野での利用を推進しており、実際にLAMP法に基づく製品は2002年以降次々と実現している。 また同様の目的から、LAMP法陣営構築のために外部に対し積極的なライセンス許諾を行っている。 LAMP法を世界的に普及させるための中心的な取り組みの一つが、「FIND」とのアライアンスである。 「FIND」は「Foundation for Innovative New Diagnostics」のことで、2003年5月に開催された国連の世界保健会議の場で設立されたスイス政府認可の非営利財団。当初5年間、Bill&Melinda Gates Foundationからの助成金を受けて活動を本格化している。 途上国における感染症撲滅のために、手頃な価格で、取り扱い易く、先進的な検査・診断方法を開発・導入する事を活動の目的としている。 FINDでは対象とする感染症として、結核、マラリア、アフリカ睡眠病などを上げているが、このうち結核について途上国で実施されている顕微鏡検査(塗沫検査)よりも精度を向上させることを目的として、LAMP法による結核検査の共同研究が同社とFINDによって2005年7月より開始された。 途上国の現場でも利用できるように、前処理工程の簡略化(PURE法)、試薬保存方法の改良(室温保存)、装置の簡略化など、PCR法では実現できない改良が加えられた。 LAMP法を利用したこの製品は2011年に日本で既に販売となっている。 現在、同社はWHO(World Health Organization、世界保健機構)の推奨獲得のために、途上国14ヵ国での臨床評価を終了し、WHOに資料を提出している。まもなく推奨を取得する見込みである。 同社は、結核以外にも前述の疾病のほか、リーシュマニア症及びシャーガス病の検査薬に関して、FINDと共同開発を進めている。 また、同社はLAMP法を利用した次世代の小型全自動遺伝子検査装置および多項目検査チップを開発している。本装置は、検体前処理(核酸抽出・精製)から増幅・検出までを全自動で行え、従来の高純度な核酸抽出・精製を行う装置と増幅・検出装置で合わせて2時間以上を要していた操作時間を、LAMP法の特徴を活かした独自プロトコルの開発により、30分以内に短縮することが可能となる。まず、複数の呼吸器感染症原因微生物の同時検出を目的とした臨床性能試験を実施するが、その使用用途は広い。 同社では、これらの製品はLAMP法の普及を加速させるとともに、新たな市場を構築した中でグローバルスタンダードとしての地位を確立させるものと期待している。 *遺伝子増幅法
遺伝子検査では、検体に含まれる目的の遺伝子量が極めてわずかなため、遺伝子を検出するためにはまず目的とする遺伝子を増幅させなければならず、遺伝子検査において最も重要なポイントが遺伝子増幅となる。
*アフリカ睡眠病
熱帯アフリカの風土病で、トリパノソーマという原虫がヒトに感染して引き起こす重大な熱帯病。ツェツェバエが媒介する。ヒトの血液中のトリパノソーマがツェツェバエに吸血され、その体内で発育、増殖し2~5週で終末トリパノソーマ型となって次の感染源となる。高熱、頭痛、嘔吐などをきたし、ひたすら眠るようになる。食事が摂れなくなるので痩せ、全身衰弱となり、多くは合併症を引き起こして死亡する。
*リーシュマニア症
リーシュマニアという原虫の感染によって引き起こされ、黒熱病といわれる内臓リーシュマニア症、皮膚と粘膜をおかすブラジルリーシュマニア症、皮膚をおかす熱帯リーシュマニア症があり、いずれも吸血昆虫、とくにサシチョウバエが媒介する。内臓リーシュマニア症は約3か月の潜伏期の後、高熱、発汗や下痢が生じ、1か月ぐらいすると肝臓と脾臓が腫れ、貧血が進み、放置すると衰弱し、半年から2年で死亡することもある。
*シャーガス病
米国南部や中南米において哺乳類吸血性であるオオサシガメ亜科のサシガメを媒介とする感染症。すぐには発病せず、一般的に30年ほどの潜伏期間がある。リンパ節、肝臓、脾臓などの腫脹、筋肉痛、心筋炎、心肥大、脳脊髄炎、心臓障害といった症状をもたらす。
|
| 2016年3月期決算概要 |
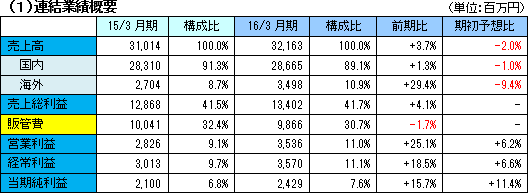 微増収・微増益。国内横這いも海外売上が好調。
売上高は前期比3.7%増の321億円。国内売上は、尿検査用試薬などが伸長した一方、便潜血検査用試薬が前年比微増、微生物検査用試薬が伸び悩み、同1.3%増であった。一方海外売上高は同29.4%増と大きく増加した。北米や欧州で便潜血検査用試薬・装置が好調だった。特にフランス、スペイン(マドリード、バルセロナ)で大腸がんスクリーニング検査が開始されたことが寄与した。 販管費のコントロールが奏功し、営業利益は同25.1%増の35億円となった。前期の為替差益が為替差損に転じたが経常利益は同18.5%増加、野木工場の新製造棟建設に伴う解体費用等1億83百万円を計上したが、当期純利益も同15.7%増加した。 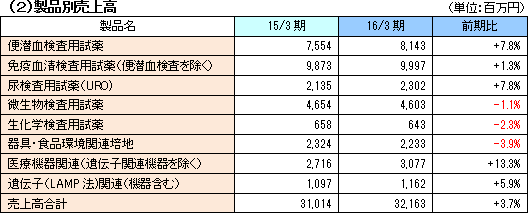 ○便潜血検査用試薬
前期比で7.8%伸長したが国内は同1.7%の微増だった。大腸がん検診普及活動による市場拡大に引き続き注力した。また、2014年11月に発売した便潜血測定装置『OCセンサーPLEDIA(プレディア)』の設置を推進し、便潜血検査用試薬の販売増を図った。一方、北米の試薬販売推進、フランス、スペイン(マドリード、バルセロナ)での大腸がんスクリーニング検査、オーストラリア、ニュージーランドでの販売拡大等で海外売上は同24.9%増となった。ただ、イングランドでの採用が遅れたため当初予想には未達となった。 ○免疫血清検査用試薬(便潜血検査を除く)
前期比1.3%増。東ソー株式会社から導入・販売している「AIA関連試薬」は前年並みだった。胃の健康度評価(ABC分類)の普及活動を推進し、ヘリコバクター・ピロリ抗体検査用のLZテストは前期比3倍となった。2016年2月に新試薬LZテストKL-6の発売を開始した。
○尿検査用試薬
前期比7.8%の増収。2015年2月に発売した全自動尿分析装置「US-3500」の新規採用先が増加し試験紙「ウロペーパーαⅢ‘栄研’」が伸長した。海外では、イタリア向け尿試験紙の販売が増加したほか、2016年1月にシスメックス社向け尿試験紙などの供給を開始した。また、新製造棟の建設を2015年11月に開始したほか、尿試験紙の新規設備導入の準備を始めた。 ○微生物検査用試薬
前期比1.1%の減収だった。生培地(ポアメディア)が減収だったことに加え、迅速検査試薬はイムノキャッチ-ノロを中心に減速した。呼吸感染症のラインアップとして2015年8月に「イムノキャッチ-RSV」、2016年1月に「イムノキャッチ-肺炎球菌」を発売した。薬剤感受性検査用試薬は売上が増加した。 ○生化学検査用試薬
前期比2.3%の減収だった。
○器具・食品環境関連培地
前期比3.9%の減収だった。
○医療機器
国内外のOCセンサーPLEDIA及び国内でのUS-3500の販売が好調で前期比13.3%の増収だった。
○遺伝子(LAMP法)関連
前期比5.9%の増収だった。LAMP製品(結核菌群、マラリア、マイコプラズマ)の試薬が伸長した。次世代の小型全自動遺伝子検査装置および多項目検査チップの開発を推進した。海外では、引き続き結核検査のWHO推奨取得に向けた活動を推進した。結核検査及びマラリアのグローバル展開のための代理店契約を準備しているほか、フィリピンでのJICA民間技術普及促進事業に結核検査が採択された。 特許料収入は前期比微減の471百万円となった。 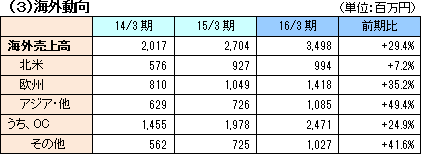 *北米
便潜血検査用試薬・装置の拡販を進めた。
*欧州
フランス、スペイン(マドリード、バルセロナ)で大腸がんスクリーニング検査が始まった。一方、イングランドは国家スクリーニングの開始が遅れている。
*アジア、その他
オーストラリア、ニュージーランドなどで便潜血検査の新規採用及び販売拡大に注力した。ASEAN、インドなどで販路拡大を図った。 中国ではLAMP製品、便潜血検査用試薬及び装置の販売促進に注力した。 *FIND事業
結核検査のWHO推奨取得に向けたWHOによるデータ分析が行われている。正式な推奨取得とは未だなっていないが、会社側は最終段階に入っていると見ている。
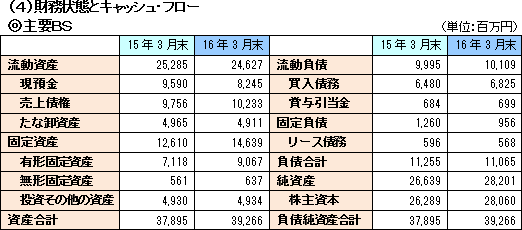 流動負債は買入債務の増加などで同1億14百万円増加した一方、固定負債は同3億4百万円減少し、負債合計は同1億90百万円減少した。 純資産は利益剰余金増などで同15億62百万円増加した。この結果、自己資本比率は前期末の69.8%から71.2%へ1.4%上昇した。 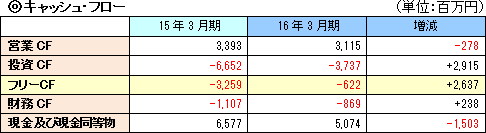 当期は長期借入金の返済が無かったため財務CFのマイナス幅も縮小した。 キャッシュポジションは低下した。 |
| 2017年3月期業績予想 |
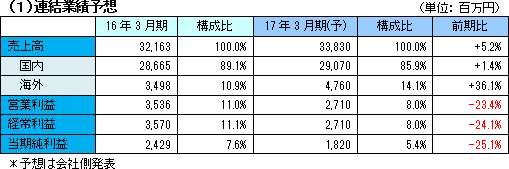 海外市場の開拓進むが、集中的な研究開発投資等により増収・減益
売上高は前期比5.2%増収の338億円の予想。欧州を中心に海外売上が今期も大きく伸長する。集中的な研究開発投資、営業活動活発化に伴う旅費、荷造費の増加、効率化推進のためのIT投資など販管費が増加し、営業利益は同23.4%減の27億円を見込む。 配当は、前期同様中間20.00円/株、期末20.00円/株の合計40.00円/株の予定。予想配当性向は40.2%。 |
| 中期経営計画(2017年3月期~2019年3月期)について |
|
【経営目標】
グローバル企業「EIKEN」の実現に向けた取り組みを加速し、ヘルスケアを通じて世界に貢献するとともに持続的な成長と着実な収益性の向上を目指す。
【業績目標】
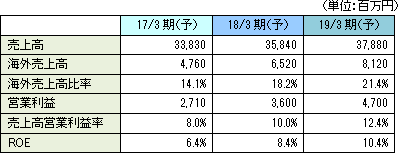 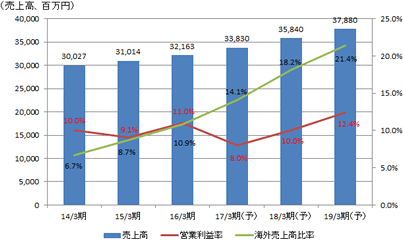 成長戦略としては、①国内市場での自社製品のシェアアップ、②グローバル展開の加速を、次の成長への投資として①研究開発の強化、②経営効率を高めるための基盤整備を掲げている。    【株主還元】
配当性向30%以上の安定した配当を目標としている。
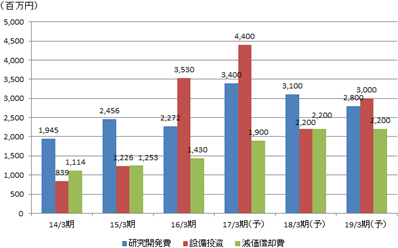
【研究開発・設備投資・減価償却】
研究開発費、設備投資とも今期2017年3月期が当面のピークとなる見込み。
 |
| 和田 守史社長に聞く |
|
「国内外とも便潜血検査試薬市場拡大の余地は大きい。海外市場開拓のための基盤再整備にも着手する。」
「自由な発想を重視する企業文化の下、コア技術を更にブラッシュアップ。新規事業や新規市場の創造にも挑戦」
「安定して利益を産み出す企業となるための基盤作りに注力する。」
|
|
| <参考:新経営構想「EIKEN WAY・EIKEN ROAD MAP 2009」> |
|
【背景】
日本国内では医療費抑制を目的とする医療制度改革の継続基調は変わることなく、診療報酬の改定、製品競争・価格競争の激化により、臨床検査関連企業には、一層の経営の効率化・合理化が求められている。加えて、安全性の確保と法令遵守が更に重要な経営課題となっており、各企業間格差が一段と大きくなると考えられる。こうした環境下、着実な成長と持続的な企業価値の向上を実現するためには長期的にEIKENグループが目指す方向性を明らかにした上で、経営資源の効率を最大化しつつ、新たな視点をもって環境変化を活かす戦略を、よりスピーディかつ大胆に進めることが必要不可欠であると同社は認識している。 そこで、同社では新経営構想として、堅実な経営を実践するためのよりどころとなる「EIKEN WAY」及び長期的な目標を見据えた「勝ち残りの経営」を推進するための基本指針となる“EIKEN ROADMAP 2009”を策定した。 【概要】
1.事業ドメイン
EIKENグループが保有する技術や強みを活かした事業領域として、『ヘルスケア』の中から「臨床検査事業」、「食品・環境検査事業」の2つを事業ドメインと定め、着実な成長と収益性向上を実現する。また、このドメインの中で次の成長を担う新規事業を創出する。
2.EIKEN ROAD MAP 2009 グランドビジョン
『2018年までに、検査のパイオニアとして人々の健康を守るため、グローバル企業“EIKEN”を実現する。』
3.EIKEN ROAD MAP 2009 行動指針
 4.基本方針
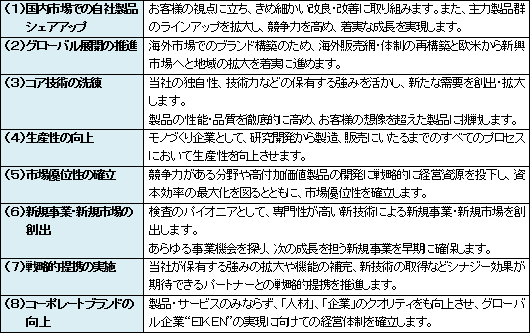 5.経営目標
世界的な検査企業入りという未来のため、強固な事業基盤作りとして着実な成長と収益性の向上を目指しており、当面は海外売上高比率10%以上の達成と連結売上高営業利益率10%以上の継続達成を目標としている。
|
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2025 Investment Bridge Co.,Ltd. All Rights Reserved. |





