ブリッジレポート:(7776)セルシード vol.22
| (7776:JASDAQ) セルシード |
|
||||||||
|
||||||||
企業名 |
株式会社セルシード |
||
社長 |
橋本 せつ子 |
||
所在地 |
東京都江東区青海二丁目5番10号 テレコムセンタービル |
||
決算期 |
12月末日 |
業種 |
精密機器(製造業) |
| 項目決算期 | 売上高 | 営業利益 | 経常利益 | 当期純利益 |
| 2014年12月 | 86 | -601 | -577 | -582 |
| 2013年12月 | 105 | -534 | -581 | -584 |
| 2012年12月 | 75 | -846 | -842 | -913 |
| 2011年12月 | 86 | -1,418 | -1,358 | -1,442 |
| 2010年12月 | 66 | -1,204 | -1,002 | -1,009 |
| 2009年12月 | 87 | -785 | -788 | -790 |
| 2008年12月 | 61 | -778 | -644 | -650 |
| 2007年12月 | 40 | -809 | -614 | -616 |
| 2006年12月 | 23 | -672 | -464 | -470 |
| 2005年12月 | 34 | -412 | -336 | -343 |
| 2004年12月 | 53 | -257 | -214 | -215 |
| 株式情報(3/1現在データ) |
|
||||||||||||||||||||||||
|
| 今回のポイント |
 |
| 会社概要 |
|
【細胞シート工学と細胞シート再生医療】
「細胞シート工学」は再生医療の汎用的なプラットフォーム技術となるもの。患者から細胞を採取し、これをシート状に培養し治療に用いるが、「細胞シート工学」の画期的なところは、温度応答性細胞培養器材を用いる事で、従来不可能だった無傷の状態での細胞回収を可能にした事だ。細胞は通常、培養皿で培養する(増殖させる)が、この場合、細胞は培養皿の表面に密着して増殖する。そして細胞を回収する際に皿から剥がすが、その際、トリプシン等のタンパク質加水分解酵素を用いて剥がすため、細胞表面のタンパク質(細胞外マトリクス)が壊れてしまい、本来の生きた細胞とは異なったものになってしまう(傷付けてしまう)。このため、これを再生医療に用いても、きちんと生着できず機能を十分に発揮できない。 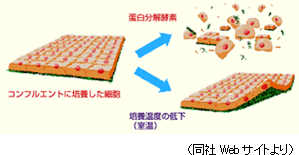
温度応答性細胞培養器材は温度を下げると、温度応答性ポリマーの性質が変わり、細胞シートが剥離するため、細胞表面のタンパク質(細胞外マトリクス)を破壊する事無く回収できる。
従来、細胞の回収に際してトリプシン等のタンパク質加水分解酵素を用いていたが、タンパク質加水分解酵素は細胞間の結合因子や接着因子を破壊し、細胞に大きな傷害を与える。 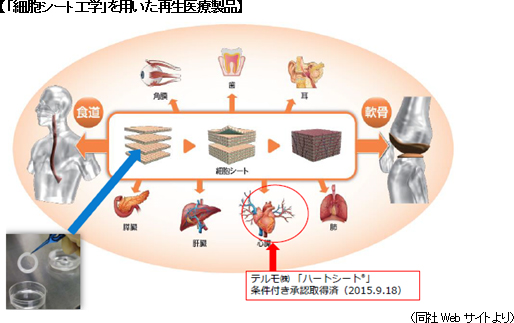 【新しい規制環境下での市場動向 -着実に進む再生医療の産業化-】
2014年11月に再生医療等製品の開発に関する法規制(「医薬品医療機器等法」、「再生医療等安全確保法」)が施行され、2015年9月には新法下の早期承認制度に基づき、テルモ製「ハートシート」(条件付き)とJCRファーマ製「テムセル HS注」(造血幹細胞移植後に発症する合併症である急性移植片対宿主病の治療製品)の2製品が承認され、それからわずか2カ月後の2016年1月に2製品の薬価基準が収載された。ちなみに、温度応答性細胞培養器材「アップセル」が組み込まれている「ハートシート」の保険償還価格(以下、価格)は、大腿部からヒト骨格筋筋芽細胞を採取する時に使用する機器の価格(キットA:6,360千円)と、細胞シート培養器材「アップセル」を含む細胞をシート状に培養する際に使用する機器の価格(キットB:1,680千円)に分けられた(治療には5枚のシートが必要となるため、総額14,760千円)。 また、2016年1月には、(株)ジャパン・ティッシュ・エンジニアリング製再生医療製品(「自家培養表皮」及び「自家培養軟骨」)の価格見直しが行われ、「ハートシート」と同様に価格がキットAとキットBに分けられた。例えば、「自家培養表皮」は重度の火傷の治療に使われる再生医療製品だが、重度の火傷のため、患者が培養中に死亡してしまうケースが多く、その場合、医療機関は皮膚細胞採取から培養に至る過程で発生した費用を回収する事ができなかった。このため、価格の見直しを行い、キットAとキットBに分けた。 自家培養表皮:4,380,000円(更に、キットAとキットBに分かれる)、自家培養軟骨:2,129,000円(同) 尚、再生医療の産業化に向けた取り組みを進める(社)再生医療イノベーションフォーラム(2011年6月設立)の会員数が183社を数える等、再生医療に対する企業の関心も高まっている。(株)セルシードは、設立以来の理事会社を務めており、同社の橋本社長が理事を務めている他、同社の社員が運営委員や国際委員として活躍している。 |
| 中期戦略の進捗状況と2015年12月期決算 |
|
(1)中期戦略(15/12期~17/12期) -細胞シート再生医療製品を開発し、世界市場への普及を目指す-
現在、細胞シート再生医療製品の開発と世界市場への普及を目指した中期戦略(15/12期~17/12期)が進行中である。具体的には、2014年11月の再生医療関連新法の施行を踏まえて日本を細胞シート再生医療開発最優先拠点と位置付け、①再生医療製品の早期事業化、及び②温度応答性細胞培養器材を中心に器材開発の促進と収益機会の拡大に取り組んでおり、③世界へ向けた事業展開も進めている。
15/12期の成果
中期戦略は15/12期から17/12期にかけての3年間を区切りとしており、その初年度となった15/12期は、再生医療製品の早期事業化、器材生産、世界展開、のそれぞれで、下記の通り、一定の成果を上げる事ができた。また、細胞培養施設(東京都江東区テレコムセンタービル内)の建設を開始した他、2015年末にはオフィスを同ビル内に移転した。 再生医療製品の早期事業化
「食道再生上皮シート」について、東京女子医科大学との開発基本合意契約を締結し、2015年12月3日に独立行政法人 医薬品医療機器総合機構(PMDA)に治験届を提出した。一方、「軟骨再生シート」についてはPMDAとの事前相談を開始し、いくつかのアドバイスを受けた他(PMDAは、治験前から承認まで一貫した体制で指導・審査を行う)、同社とDNAチップ研究所が共同で提出した軟骨再生シート関連の提案が国立研究開発法人 日本医療研究開発機構(AMED)の評価方法に関するプロジェクトに採択された。尚、「食道再生上皮シート」については、PMDAとの質疑応答の中で、いくつかの変更点が出てきたため、2015年12月24日に治験届を取り下げた。2016年4月前後に再提出する予定である。当初の予定症例数よりも少数例での治験実施が可能と判断できた事に加え、実施中の非臨床試験について、試験成績の取得等を含めて一部見直しの必要が生じたと言う。 器材生産(大日本印刷への委託による)
大日本印刷での器材の生産が軌道に乗り、委託生産が本格化した他、認知度向上を目的に展示会への出展や顧客訪問を積極的に行った。大日本印刷とは開発面でも連携を深め、新製品開発につなげていく考え。
世界に向けた事業展開
昨年5月にスウェーデンに子会社を設立し、「食道再生上皮シート」に関してスウェーデン医薬品庁(日本のPMDAに相当)との相談を開始した他、国際幹細胞学会(ISSCR)に参加する等、現地での活動を活発化させた。
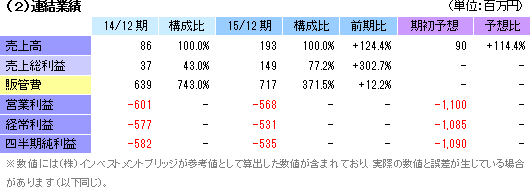 売上高193百万円、営業損失568百万円。ほぼ修正予想に沿った着地
2015年12月24日に業績予想を修正しており(修正値:売上高200百万円、営業利益△570百万円、経常利益△550百万円、当期純利益△555百万円)、修正値に沿った着地となった。売上面では、米国Emmaus Medical Inc.との間で2011年4月に締結した「米国における角膜再生上皮シート共同開発・事業化契約」及び「共同研究開発基本契約」の終結を決定した事に伴い、2012年3月に受領した一時金のうち前受金勘定としていた113百万円を売上計上した(上方修正の要因となった)他、再生医療支援事業で温度応答性細胞培養器材の売上80百万円を計上した。 利益面では、上記の売上の上振れに伴う利益の上振れに加え、細胞培養施設(2016年夏頃の稼働を予定)の準備計画の短縮化による一部費用削減及び本社機能管理費用等の節減による費用減少約150百万円、更には優先的に自社開発を進めている細胞シート再生医療パイプラインである食道上皮再生シートの日本及びスウェーデンにおける開発関連費用等250百万円の計上先送りが上方修正要因である。尚、研究開発費は3億02百万円と前期に比べて53百万円増加した。 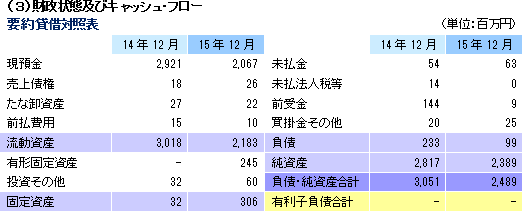  |
| 中期戦略の下で進める中期経営計画(16/12期~18/12期) |
 【再生医療製品の早期事業化】
食道再生上皮シート
食道がん再生治療法(食道創傷治癒・狭窄予防)として東京女子医大先端研が開発した治療法である。患者から採取した口腔粘膜から細胞を取り出し、取り出した細胞を同社の細胞培養施設CPCに持ち込み、温度応答性培養器材を用いて約2週間かけて細胞を培養し、細胞シートを作成する。細胞シートの培養に合わせて、食道がん切除内視鏡手術を行い、食道潰瘍面に移植する。
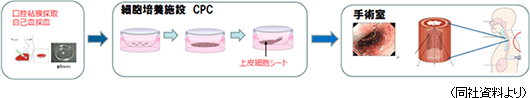 30症例の臨床研究
2008年から2014年にかけて大学で臨床研究が行われ、既に、東京女子医科大学10症例、東京女子医科大学・長崎大10症例(長距離輸送検証:長崎大で採取した細胞を東京女子医大で培養し、長崎大で移植手術)、カロリンスカ大学病院(スウェーデン)10症例、の計30症例がある。
企業治験・販売承認申請に向けた取り組み
同社は、東京女子医科大学と開発基本合意契約を締結し、同大学の研究成果を引き継いだ。既に説明した通り、PMDA薬事戦略相談を終了し、2015年12月3日に治験届を提出したが、届出後のPMDAとの質疑応答の中で、いくつかの変更点が出てきたため、2015年12月24日に治験届を取り下げた。2016年4月前後に再提出する予定である。また、海外では、スウェーデンでの企業治験を計画しており、その推進役となる子会社CellSeed Sweden AB(スウェーデン)を2015年5月に設立し、2015年11月30日にはスウェーデン医薬品庁(MPA)に事前相談を行った。欧州全体での承認を目指して、現在、欧州医薬品庁(EMA)との事前相談に向けた準備を進めている。 軟骨再生シート
軟骨再生シートは、東海大学整形外科佐藤正人教授との共同研究であり、スポーツによる損傷や加齢を原因とする軟骨欠損や変形性関節症を適応症とする(いずれも、現在、根治する方法がない)。軟骨細胞を培養して作製した細胞シート(3枚重ねた積層化軟骨再生シート)を患部に移植し、軟骨表面を根本的に再生する。既に事前相談が始まっており、PMDAからアドバイスを受けているが、更に相談を重ね、安全性データの蓄積と臨床プロトコルの確立に取り組んでいく。尚、膝の軟骨は、硝子(しょうし)軟骨と言い、耳や鼻等の軟骨とは異なり、クッション性と対摩耗性に優れた硬い軟骨だ。同社の軟骨再生シートは、硝子軟骨として膝の軟骨を再生できる事が特徴である。 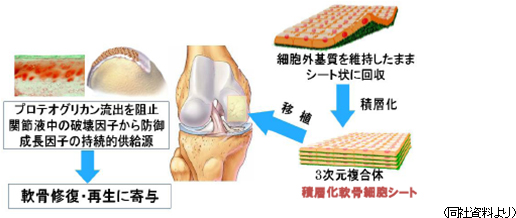 【再生医療支援事業を拡充し、収益機会を拡大】
既存製品の応用範囲の拡大や新製品の開発で収益機会を拡大させると共に、営業手法を多様化していく。現在、温度応答性細胞培養器材として、「アップセル」、「レプセル」、及び「ハイドロセル」という3製品を有するが、これら3製品の応用範囲を広げると共に新しい製品の開発を進める他、臨床応用向けの製品開発にも取り組んでいく。また、営業手法の多様化では、販売後の技術サポートに力を入れ、新しい研究への応用を支援すると共に、より使いやすい製品等、新製品の開発につなげていく他、展示会やセミナーを開催して説明機会を増やし、認知度向上につなげていく。この他、国内外の販売網も強化・拡充する。 【国内・海外の組織体制】
国内
本社をテレコムセンタービル15階(東京都江東区青海)に移転し、2016年1月より新本社で業務を開始した。また、同ビルの6階では自社細胞培養施設の新設工事が進行中である。CPC4ラインを持つクリーンルームであり、延べ床面積は約763㎡。春頃には設備が完成し、その後のバリデーション作業(製造手順の検証作業)を経て今夏に稼働する予定である。この他、東京女子医科大学先端生命医科学研究所内にある、CPC1ラインにて食道治験用細胞シートを製造する予定であり、東京女子医科大学先端生命医科学研究所とは引き続き密接な連携を取っていく考え。 欧州
既に説明した通り、食道再生上皮シートの欧州での販売承認に向け、2015年5月にCellSeed Sweden ABを設立した。欧州では、2008年10月にCellSeed France SARL(仏)を、2010年6月にはCellSeed Europe Ltd.(英)を、それぞれ設立しており、CellSeed SwedenABを含めた3拠点体制の下、欧州全域で細胞シート再生医療事業を展開していく。
【資金調達の状況】
自社細胞培養施設の準備・運営資金、再生医療支援事業関連仕入、及び国内外での業務推進のための運転資金確保を目的に、2015年8月31日、第三者割当方式により新株予約権を発行した。
第13回新株予約権
 |
|
| 本レポートは情報提供を目的としたものであり、投資勧誘を意図するものではありません。また、本レポートに記載されている情報及び見解は当社が公表されたデータに基づいて作成したものです。本レポートに掲載された情報は、当社が信頼できると判断した情報源から入手したものですが、その正確性・完全性を全面的に保証するものではありません。当該情報や見解の正確性、完全性もしくは妥当性についても保証するものではなく、また責任を負うものではありません。 本レポートに関する一切の権利は(株)インベストメントブリッジにあり、本レポートの内容等につきましては今後予告無く変更される場合があります。 投資にあたっての決定は、ご自身の判断でなされますようお願い申しあげます。 Copyright(C) 2025 Investment Bridge Co.,Ltd. All Rights Reserved. |





